免疫學新發現!國內第3重大傷病「自體免疫疾病」 國衛院發現關鍵致病機轉
根據衛生福利部統計,自體免疫疾病是國內10大重大傷病的第3名、也是門診第3常見疾病,目前尚無法治癒。國衛院11日發表最新研究成果,表示研究發現自體免疫疾病關鍵致病機制,未來將以磷酸酶 DUSP22 與泛素酶UBR2 ,作為新藥物開發標靶。
所謂自體免疫疾病,是一種人體內的免疫系統異常活化而攻擊自己身體器官的疾病,例如全身性紅斑狼瘡(SLE)、僵直性脊椎炎(AS)、類風濕關節炎(RA)等。這些自體免疫疾病目前尚無法治癒,病患必須終生接受治療與用藥,飽受病痛之苦,承受藥物引發的副作用,因此治療自體免疫疾病是醫界長久以來的挑戰。
對此,國衛院免疫醫學研究中心特聘研究員譚澤華、副研究員莊懷佳率領的研究團隊,在歷經6年探索,終於成功解開去磷酸酶DUSP22缺失促使泛素酶UBR2含量上升,引發T淋巴細胞過度活化導致自體免疫疾病的關鍵致病機制。
2014年,團隊首度發現去磷酸酶DUSP22是負責抑制T細胞過度活化以及自體免疫反應的關鍵負調控分子,接續與台中榮民總醫院陳一銘醫師、台北榮民總醫院免疫風濕科陳明翰醫師合作,研究自體免疫疾病SLE及AS致病成因與精準之生物診斷標記,分析臨床檢體發現,SLE及AS患者體內T淋巴細胞中的去磷酸酶DUSP22表現量與正常T細胞相比大幅下降,且與疾病嚴重度相關。
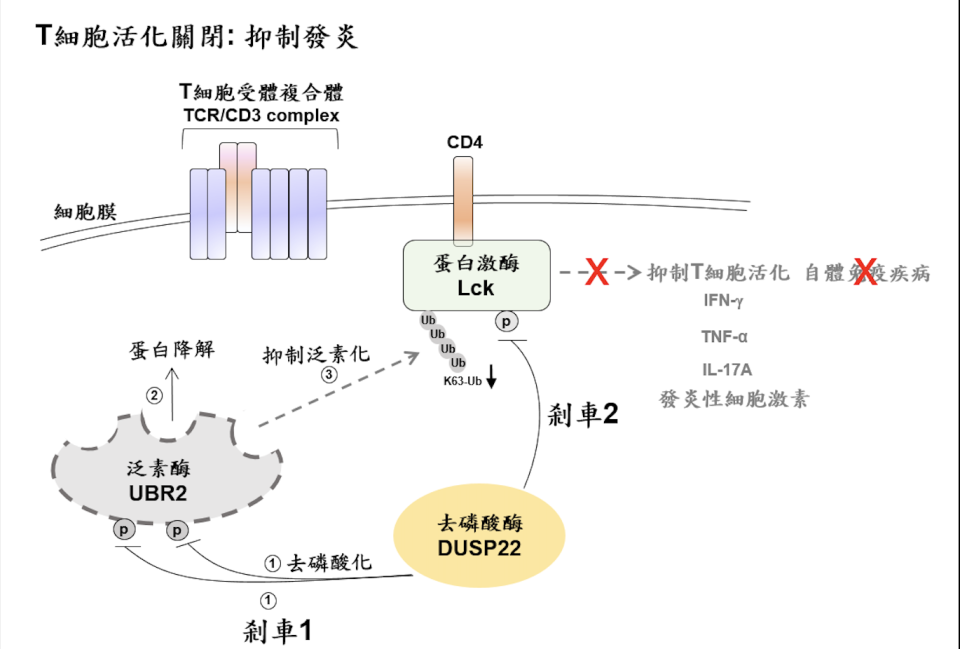
團隊指出,去磷酸酶DUSP22的缺乏造成蛋白激酶Lck異常地持續活化,促使T淋巴細胞大量分泌發炎性細胞激素,正是造成自體免疫疾病的元凶。
研究團隊進一步運用蛋白質體學、單細胞RNA定序…等大數據分析,結合基因改造小鼠及各種生化實驗分析,發現泛素酶UBR2實為蛋白激酶Lck的上游活化分子,UBR2會誘使Lck泛素化並且促使Lck活化,這也是免疫學界從未觸及的嶄新發現。
研究人員證實,去磷酸酶DUSP22在正常T淋巴細胞中,會透過「雙重剎車手續」徹底解除T細胞之活化狀態,以避免過度活化引發疾病。第一道煞車是:DUSP22可以直接將泛素酶UBR2去磷酸化並引發UBR2蛋白質降解;第二到煞車即:DUSP22也會將已活化的蛋白激酶Lck去磷酸化並抑制Lck活性。因此當T淋巴細胞中缺乏DUSP22時,泛素酶UBR2蛋白質會過度累積,進而使蛋白激酶Lck泛素化增加且持續性地活化,就如同高速行駛的跑車完全失去剎車功能一般,導致一發不可收拾的發炎反應。
分析SLE患者的臨床檢體顯示,患者T淋巴細胞中泛素酶UBR2表現量增加,UBR2與Lck結合及Lck之泛素化也增加,證實去磷酸酶DUSP22的缺失及泛素酶UBR2上升為自體免疫疾病致病機轉的關鍵因素。研究團隊近一步運用DUSP22及UBR2基因剔除小鼠進行自體免疫反應實驗,發現原本因DUSP22缺失所誘發大量產生的發炎性細胞激素,在進一步剔除泛素酶UBR2基因時,小鼠體內的發炎性細胞激素含量下降,且發炎情況大幅降低。
這項重大的發現,證實去磷酸酶DUSP22與泛素酶UBR2在T淋巴細胞的活化中扮演極重要的角色,將有助於開發新穎的醫療策略,研究成果已在2024年1月發表於全球知名期刊《Nature Communications》。國衛院強調,抑制 T 淋巴細胞中表現量或活性,未來將是一種做為緩解自體免疫疾病的新思維,可以為自體免疫疾病的醫療策略帶來新的方向。

 Yahoo奇摩新聞
Yahoo奇摩新聞 